LES
REACCIONS REDOX IMPLICADES EN UNA PILA ALCALINA.
Les piles
alcalines, o també
anomenades de tipus
Mallory, són
probablement les més utilitzades en l’actualitat, a pesar que
estan sent desplaçades en molts aparells
electrònics (telèfons mòbils, cambres,
reproductors de música i vídeo…) per les bateries recarregables.
Qui no recorda al conillet de Duracell i al conegut eslògan “i
duren, i duren, i duren…”?
Doncs bé, una pila alcalina es fonamenta en la reacció d’oxidació reducció que es dóna entre el zinc metàl·lic i el diòxid de manganés al mig bàsic (d’ací el nom d’alcalina). Com a electròlit conté hidròxid de potassi, KOH, que és el que aporta el medi bàsic requerit per la reacció i la migració de la qual evita la polarització de la pila (recorda que era necessari un electròlit dins del pont salí per al funcionament de qualsevol cel·la electroquímica).
En l’ànode,
és a dir, en
l’elèctrode de polaritat negativa, es produïx l’oxidació del
Zn polvoritzat, mentre
que en el càtode, és
a dir, en l’elèctrode de polaritat positiva, es produïx la
reducció de l’òxid
de manganés (IV),
MnO2,
(que actua com a oxidant) per a donar òxid de manganés (III),
Mn2O3.
Les semirreacciones
que es produïxen són les següents:
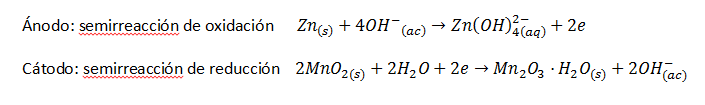

Com veus, són unes
semirreacciones
més complicades que les que hem vist en l’ajust
de reaccions d’oxidació-reducció
del temari. Ni tan sols les semirreacciones
indicades descriuen per complet el procés real,
són una simplificació del mateix, que transcorre en diverses etapes
amb formació de distints compostos intermedis. A més, les
semirreacciones
no transcorren, com hem vist, en dissolució. En una pila alcalina,
l’ànode
està format per zinc
polvoritzat, i el
càtode
és una barra d’acer
rodejada d’una pasta espessa
i negrosa de MnO2,
KOH i aigua.
Es produïxen multitud
de reaccions paral·leles en funció de les condicions de l’entorn.
Per exemple, la reacció de producció d’hidrogen. Has vist alguna
vegada una pila alcalina inflada com un globus, com a punt
d’explotar?. Es deu a la següent reacció secundària:
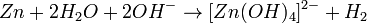
que produïx
hidrogen gasós i la fa inflar-se.
El procés
global d’una pila
alcalina es pot
escriure com:
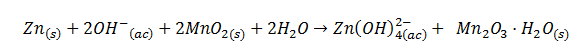
Ací tens una
fotografia on es mostren l’ànode (la carcassa exterior) i el
càtode (el cilindre central):
Cap comentari:
Publica un comentari a l'entrada